医療関係者の方へ
2019年9月、長崎大学病院は、厚生労働省より「がんゲノム医療拠点病院」に指定されました。
当院では、保険診療による検査『OncoGuide™ NCCオンコパネルシステム』・『FoundationOne® CDx がんゲノムプロファイル』・『FoundationOne® LiquidCDxがんゲノムプロファイル』・『GenMine TOPがんゲノムプロファイル』・『Guardant360 CDxがん遺伝子パネル』を行っています。
当院では、保険診療による検査『OncoGuide™ NCCオンコパネルシステム』・『FoundationOne® CDx がんゲノムプロファイル』・『FoundationOne® LiquidCDxがんゲノムプロファイル』・『GenMine TOPがんゲノムプロファイル』・『Guardant360 CDxがん遺伝子パネル』を行っています。
受診のためのお申し込みについて
| ● | 長崎大学病院の医療従事者の方へ |
|---|---|
| 下記3点の記入とお手続きをお願い致します。 |
|
|||
| ご不明の際は下記までご連絡ください。 | |||
|
| ● | 当院にご紹介される医療機関関係者の方へ |
|---|
|
| 当科ご紹介にあたり、院外患者さんの検査に必要なもの | |
|---|---|
|
| 組織検体について | |
|---|---|
| 当院以外で保管されている標本で提出される場合の検体提出の流れについて、ご紹介前に下記のPDFを確認してください。 | |
| 当院以外に保管されている組織検体の遺伝子パネル検査提出の流れ  (PDF) (PDF) |
遺伝子パネル検査を受けるにあたり、検査を依頼されてから検体を検査会社へ提出するまでの流れは下記の通りです。
|
提出する組織検体の選定について
当院の病理医が検体確認の際に、各検査の規定を基に提出検体としての適性や未染スライドの枚数を確認します。
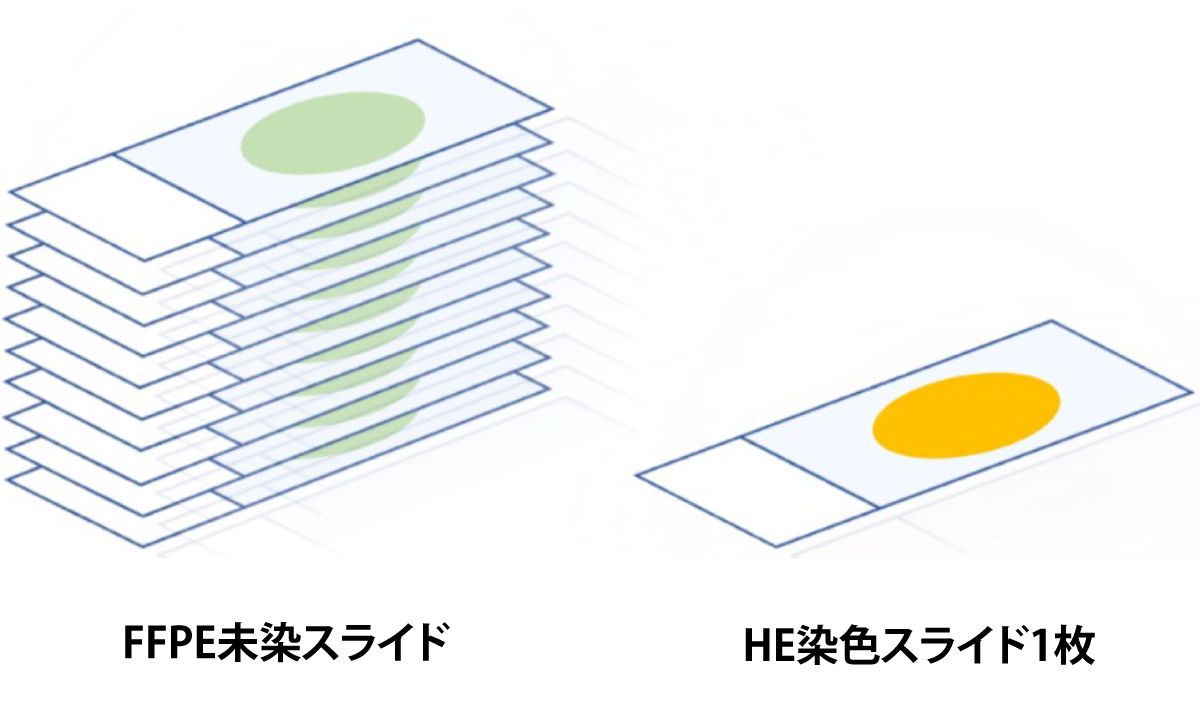
検査時の提出物
- HE染色スライド1枚+FFPE未染スライド
| 検査名 | FoundationOne® CDx |
OncoGuide™ NCCオンコパネルシステム |
GenMine TOP |
|---|---|---|---|
| 未染スライド枚数・切片の厚さ | 10枚以上(厚さ4~5㎛) | 5枚程度(厚さ10㎛) 10枚程度(厚さ5㎛) |
16枚以上(厚さ5㎛) 8枚以上(厚さ10㎛) |
| 有核腫瘍細胞割合 (マイクロダイセクション後) |
最適:30%以上 最低:20%以上 |
20%以上 | 20%以上 |
| 表面積・合計体積 |
|
|
|
| その他注意事項 |
|
|
|
各検査の検体作製についての詳細は、下記のリンクよりご確認ください。
| スライド作製時の注意点 |
|---|
| ※匿名で検査会社へ提出するため、全てのスライドのフロスト部分には同一の検体番号のみを(鉛筆で手書きするなどして)記載してください。 |
検査精度に影響を与える要因
(参考)一般社団法人 日本病理学会 ゲノム診療用病理組織検体取扱い規定 
|