臨床研究(倫理指針)
他の倫理審査委員会で審査を受ける場合
(研究実施許可の手続き)
手続きはすべてCTポータルからお願いします。
長崎大学病院のみの単機関、あるいは長崎大学病院が代表機関の多機関共同研究を長崎大学病院臨床研究倫理委員会以外の倫理委員会で審査する場合は事前に臨床研究センター 管理ユニット(内線:7726)へご連絡ください。
審査依頼前の確認事項
事前に病院長の承認や許可を得る必要はありません。
- 審査を行う倫理委員会が、倫理指針に準拠して設置されていること
- 研究責任者、分担者に十分に研究を実施する時間的余裕があること
- 当院が当該研究の実施要件を満たしていること
(実施体制や人員、事務的な手続きも含む) - 当院の研究責任者、研究分担医師が研究者の要件を満たしていること
実施許可手続きに必要な資料の準備
倫理審査委員会の承認が得られたら、長崎大学病院において研究実施の手続きを行います。
長崎大学病院の研究責任者は研究代表者から研究承認の連絡を受けた場合、速やかに研究実施許可の手続きを行ってください。
長崎大学病院で研究を行うには、倫理審査委委員会の承認と病院長の許可が必要です。
【実施許可手続きに必要な資料】
- 研究計画書
⇒ 研究代表者から提供された研究計画書をそのまま提出 - 長崎大学病院が審査対象機関であることがわかる資料
- 長崎大学病院が共同研究機関であることがわかる資料(多機関共同研究の場合)
- 同意説明文書あるいは情報公開文書(下記の両方の文書の添付が必要です)
- 倫理審査委員会で承認された文書
- 理審査委員会で承認された文書を元に研究責任者名や連絡先を長崎大学病院用に修正したもの
- 審査結果通知書
- その他、別紙、添付資料として取り扱われる資料
- 長崎大学病院用の文書は、別途長崎大学病院用の作成日、版数をつけてください。
(もともとの文書に記載してある作成日、版数は削除しないこと)
研究実施許可の手続き
倫理審査員会の承認だけで研究を開始する事はできませんのでご注意ください。
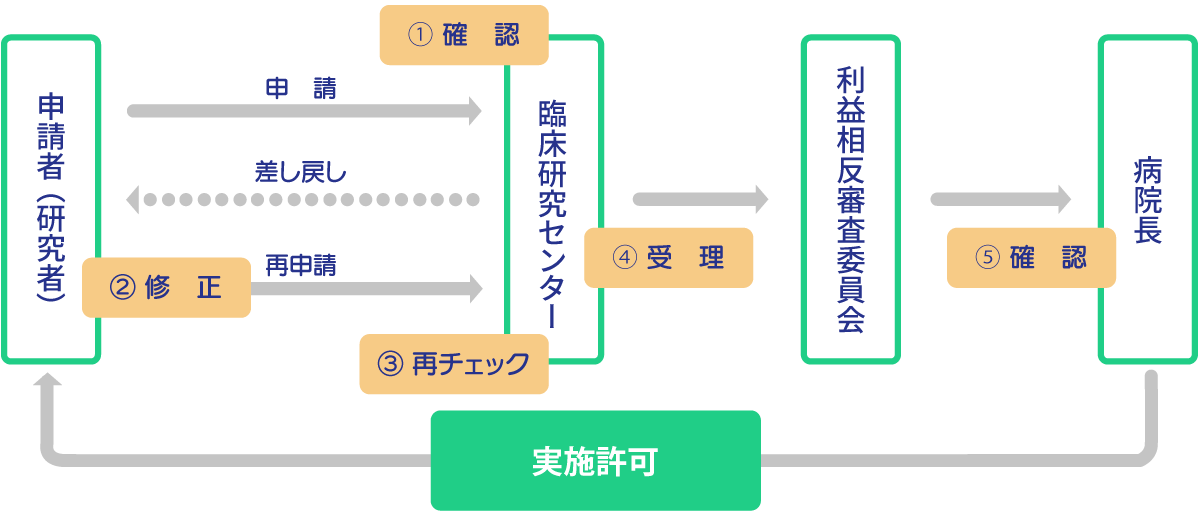
| 実施許可の流れ | |
|---|---|
| ① |
必要な書類が提出されているのを確認したら、臨床研究センターが申請内容を確認します。
【臨床研究センターからの確認書について】
|
| ② | 差し戻しの内容を確認し、修正等を行い、再申請してください。 (システム上の申請状況の表示は「申請NG」) 差し戻しの内容はCTポータルの「申請情報一覧」⇒「課題名」⇒「コメント履歴」から確認できます。 |
| ③ |
|
| ④ | 確認が終わったら、利益相反管理委員会で利益相反の確認します。 (システム上の申請状況の表示は「申請受理」) |
| ⑤ |
研究の実施について病院長が必要と判断した場合は倫理審査委員会へ実施の可否について諮問する場合があります。(二重審査には該当しません)
|
研究実施中の手続き
- 研究計画書に従って実施すること
(研究計画書に記載されていないことは実施しない) - 病院長が許可した範囲(申請書の記載内容)を超えて研究を実施しないこと
(例:症例数や研究分担者、その他、研究計画書等に記載がなく、確認書や補遺を元に許可した内容) - 研究計画に変更が生じる場合は、変更が生じる前に変更申請の手続きを行うこと
- 研究の進捗状況は随時確認し、申請した症例数を超えないように管理すること
- 人事異動などに伴う研究者(特に研究責任者)の不在や研究者以外の研究行為が行われないように管理すること
研究代表者より研究全体の実施状況報告を受けた場合は、長崎大学病院の実施状況と併せて報告してください。
研究開始から一年以上経過しても研究代表者より実施状況報告が届かない場合は、倫理審査委員会への報告状況を研究代表者へ確認してください。
○ 手続きに必要な資料は コチラ ![]()
研究者等は、侵襲を伴う研究の実施において重篤な有害事象の発生を知った場合には研究代表者、倫理審査委員会、病院長への報告が必要です。
研究計画書、手順書に従い、速やかに報告してください。
実施された研究との因果関係の有無を問わず、研究対象者に生じた全ての好ましくない又は意図しない傷病若しくはその兆候(臨床検査値の異常も含む)
有害事象のうち、次に掲げるいずれかに該当するものをいう。
- 死に至るもの
- 生命を脅かすもの
- 治療のための入院または入院期間の延長が必要となるもの
- 永続的又は顕著な障害・機能不全に陥るもの
- 子孫に先天異常を来すもの
当院で発生した事象と他機関で発生し事象の申請区分が異なるのでご注意ください。
不適合・逸脱の発生を知った場合は、当院、他院発生事例問わず、速やかに臨床研究センター管理ユニットへ連絡してください。
研究代表者より研究計画書の変更について連絡を受けた場合は速やかに病院長へ実施許可の手続きを行ってください。
下記のような変更申請が生じた場合は研究代表者へ報告し、必要な手続きについて確認をお願いします。
- 研究責任者の変更
- 研究分担者の変更
- 診療科、部門の名称変更
- 組織改編等による連絡先の変更
○ 手続きに必要な資料は コチラ ![]()
研究代表者から当該研究終了の連絡を受けたら、研究終了(中止)の報告を病院長宛に行なってください。
○ 手続きに必要な資料は コチラ ![]()
研究に用いられた試料・情報は研究代表者の指示あるいは研究計画書に定めた方法に従って保管してください。
研究者が異動、退職した後も研究計画に定められた期間までは定められた場所での保管義務が生じます。
予めご了承ください。

